提起鉆石,你可能會想到光彩奪目、閃爍耀眼的精美飾品,以及它昂貴的價(jià)格;提起石墨,你可能會想到黑乎乎、滑膩膩的碳棒。純凈的金剛石是無色透明、正八面體形狀的固體;石墨是一種深灰色有金屬光澤而不透明的細(xì)鱗片狀固體。石墨很軟,在紙上畫過可留下痕跡,有滑膩感。金剛石和石墨“形”或“性”有著天壤之別,但它們具有相同的“質(zhì)”,它們是一對“孿生”兄弟,都由碳元素組成,被稱“同素異形體”。
金剛石可以用來切割玻璃、做鉆頭,因?yàn)樗挠捕群艽螅皇梢杂脕碜鲢U筆芯、潤滑劑,這是因?yàn)樗苘洝⒂谢伕小0凑漳嫌捕葮?biāo)準(zhǔn),金剛石為最高級。金剛石是自然界中天然存在的最堅(jiān)硬的物質(zhì)。金剛石和石墨同樣由碳原子構(gòu)成,金剛石為什么會如此的堅(jiān)硬,這取決于它的分子結(jié)構(gòu)。
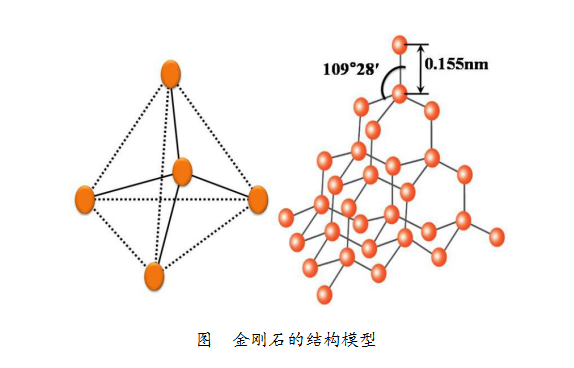
下圖是金剛石的結(jié)構(gòu)模型。每個(gè)碳原子都與周圍的4個(gè)碳原子通過強(qiáng)烈的相互作用緊密結(jié)合。“緊密結(jié)合”的兩個(gè)碳原子之間的距離約為0.155nm,從而形成致密的三維結(jié)構(gòu),正是這種致密的結(jié)構(gòu),使得金剛石成為天然存在的最堅(jiān)硬的物質(zhì)。
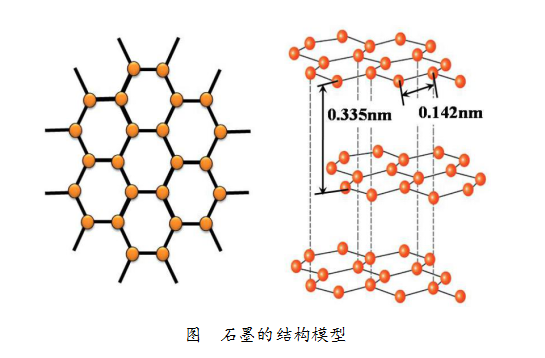
而石墨是層狀的結(jié)構(gòu),就一個(gè)片層而言,每1個(gè)碳原子會與其周圍的3個(gè)碳原子通過強(qiáng)烈的相互作用緊密結(jié)合,“緊密結(jié)合”的兩個(gè)碳原子之間的距離約為0.142nm。在石墨中層與層之間相距為0.335nm,由于距離比較大,碳原子的相互作用較弱,因此很容易沿著與層面平行的方向滑動、裂解,所以石墨很軟、有滑膩感。
金剛石和石墨相比,結(jié)構(gòu)更為致密。金剛石的密度大約是石墨的1.5倍左右(金剛石的密度約為3.5-3.53g/cm3,石墨的密度約為2.09–2.23g/cm3)。
碳原子通過強(qiáng)烈的相互作用(化學(xué)鍵)緊密結(jié)合時(shí),原子間的距離越小,相互作用越強(qiáng)。在石墨的一個(gè)片層中,碳原子間的距離比金剛石小,相互作用更強(qiáng),更難被破壞,所以石墨的熔點(diǎn)更高。
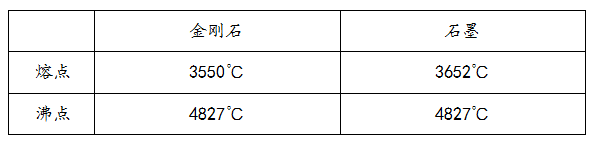
如下表所示,金剛石和石墨的熔點(diǎn)不同,但沸點(diǎn)卻相同,這又是為什么呢?物質(zhì)的物態(tài)變化與微粒間的距離是有一定關(guān)系的。石墨和金剛石熔化以后,碳原子原來的排列方式被打破,原子間的距離相等,相互作用強(qiáng)度也相同,所以沸點(diǎn)相同。
我們都知道,石墨具有導(dǎo)電性。這與石墨的結(jié)構(gòu)也有密切關(guān)系。碳原子最外層有4個(gè)電子,在石墨的一個(gè)片層中,每個(gè)碳原子會與其周圍的3個(gè)碳原子通過“共用電子對”形成強(qiáng)烈的相互作用(化學(xué)鍵),每個(gè)碳原子只有3個(gè)最外層電子參與這種“力”的形成,這樣就會剩下1個(gè)自由電子。因?yàn)橛写罅孔杂呻娮哟嬖冢允軐?dǎo)電。而金剛石中每個(gè)碳原子與其周圍的4個(gè)碳原子通過“共用電子對”形成強(qiáng)烈的相互作用,碳原子最外層的4個(gè)電子幾乎都參與了這種“力”的形成,基本沒有自由電子,所以基本不導(dǎo)電。
結(jié)構(gòu)可以決定性質(zhì),金剛石和石墨都由碳原子構(gòu)成,但是因?yàn)樵优帕蟹绞讲煌瑢?dǎo)致很多物理性質(zhì)有很大差異。


